Сера в природе известна в нескольких полиморфных кристаллических модификациях, в коллоидных выделениях, в жидком и газообразном состояниях. В природных условиях устойчивой модификацией является ромбическая сера (α-сера). При атмосферном давлении при температуре выше 95,6° α-сера переходит в моноклинную β-серу, при охлаждении снова становится ромбической. γ-сера также кристаллизующаяся в моноклинной сингонии, при атмосферном давлении неустойчива и переходит в α-серу. Структура γ-серы не изучена; в данную структурную группу она отнесена условно.
В статье рассмотренно несколько полиморфных модификаций серы: α-сера, β-сера, γ-сера
α-модификация
Английское название минерала α-сера - α-Sulрhur
Происхождение названия
Название α-сера введено Дана (1892).
Синонимы:
Ромбическая сера. Обычно просто называется серой. Дэйтон-сера (Сузуки, 1915) - псевдоморфоза α-серы по β-сере.
Формула
Химический состав
Нередко самородная сера является практически чистой. Сера вулканического происхождения часто содержит небольшие количества As, Se, Те и следы Тi. Сера многих месторождений загрязнена битумами, глиной, разными сульфатами и карбонатами. В ней наблюдаются включения газов и жидкости, содержащей маточный раствор с NaCl, СаСЬ, Na2SO4 и др. Содержит иногда до 5,18% Se (селенистая сера)
Разновидности
1. Волканит
- (селенистая сера) оранжево-красного, красно-бурого цвета.
 Кристаллографическая характеристика
Кристаллографическая характеристика
Сингония. Ромбическая.
Класс. Дипирамидальный. Некоторые авторы считали, что сера кристаллизуется в ромбо-тетраэдрический класс так как иногда она имеет вид сфеноидов, но эта форма, по Руайе, объясняется влиянием асимметрической среды (активных углеводородов) на рост кристаллов.
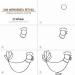
Кристаллическая структура серы
Структура серы молекулярная: 8 атомов в решетке входят в одну молекулу. Молекула серы образует восьмерные кольца, в которых атомы чередуются на двух уровнях (вдоль оси кольца). 4 атома S одного уровня образуют квадрат, повернутый относительно другого квадрата на 45°. Плоскости квадратов параллельны оси с. Центры колец располагаются в ромбической ячейке по «алмазному» закону: в вершинах и центрах граней гранецентрированной ячейки и в центрах четырех октантов из восьми, на которые делится элементарная ячейка. В структуре серы выдержан принцип Юма-Розери, требующий для элементов менделеевской группы V1б координации 2 (= 8 - 6). В структуре теллура - селена, а также в моноклинной сере это достигается спиральным расположением атомов, в структуре ромбической серы (а также синтетических β-селене и β -теллуре) - их кольцевым расположением. Расстояние S - S в кольце равно 2,10 А, что в точности совпадает с расстоянием S - S в радикале S 2 пирита (и ковеллина) и немного больше расстояния S-S между атомами S из разных колец (3,3 А).
Форма нахождения в природе
Облик кристаллов
Облик кристаллов различный - дипирамидальный, реже толстотаблитчатый по с (001), дисфеноидальный и др. На гранях (111) наблюдаются фигуры естественного травления, отсутствующие на гранях (113).
Двойники
Редки двойники по (101), (011), (110) или (111), отмечаются также двойники по (211).
Агрегаты. Сплошные массы, шаровые п почковидные выделения, сталактиты и сталагмиты, порошковатые налеты и кристаллы.
Физические свойства
Оптические
- Цвет серно-желтый, соломенно- и медово-желтый, желто-бурый, от примесей красноватый, зеленоватый, серый; иногда от примесей битумов цвет коричневый или почти черный.
- Черта бесцветная.
- Блеск алмазный
- Отлив смолистый до жирного.
- Прозрачность. Прозрачна до просвечивающей.
Механические
- Твердость 1-2. Хрупка.
- Плотность 2,05-2,08.
- Спайность по (001), (110), (111) несовершенная. Отдельность по (111).
- Излом раковистый до неровного.
Химические свойства
Растворяется в сероуглероде, скипидаре, керосине.
Прочие свойства
Электропроводность при обычной температуре почти равна нулю. При трении сера электризуется отрицательно. В ультрафиолетовых лучах пластинка толщиной 2 мм непрозрачна. При атмосферном давлении температура плавл. 112,8°; температура кипения + 444,5°. Теплота плавления при 115° 300 кал/г-атом. Теплота испарения при 316° 11600 кал/г-атом. При атмосферном давлении при 95,6° α-сера переходит в β-серу с увеличением объема.

Искусственное получение
Получается путем возгона или кристаллизацией из раствора.
Диагностические признаки
Легко узнается по желтому цвету, хрупкости, блеску и легкости воспламенения.
Сопутствующие минералы. Гипс , ангидрит , опал , ярозит , асфальт, нефть, озокерит, газообразный углеводород, сероводород, целестин , галит , кальцит , арагонит , барит , пирит.
Происхождение и нахождение в природе
Самородная сера встречается только в самой верхней части земной коры. Образуется при разнообразных процессах.
Большую роль в образовании месторождений серы играют животные и растительные организмы, с одной стороны, как аккумуляторы S, а с другой, как способствующие распаду H 2 S и других сернистых соединений. С деятельностью бактерий связывают образование серы в водах, илах, почвах, болотах и в нефтях; в последних она частью содержится в виде коллоидных частиц. Сера может выделяться из вод, содержащих H 2 S, под влиянием кислорода воздуха. В приморских районах местами сера выпадает при смешении пресной воды с соленой (из H 2 S морской воды, под действием кислорода, растворенного в пресных водах). Из некоторых природных вод сера выделяется в виде белой мути (р. Молочная в Куйбышевской обл, и др.). Из вод серных источников и из болотных вод, содержащих H 2 S и S, сера выпадает в северных районах России в зимний период в процессе вымораживания. Главным источником образования серы во многих месторождениях так или иначе является H 2 S, какого бы происхождения он ни был.
Значительные скопления серы наблюдаются в вулканических областях, в зоне окисления некоторых месторождений и среди осадочных толщ; месторождения последней группы служат основными источниками самородной серы, добываемой для практических целей. В вулканических областях сера выделяется как при извержениях вулканов, так и из фумарол, сольфатар, горячих источников и газовых струй. Иногда из кратера вулкана выливается расплавленная масса серы в виде потока (в Японии), причем сначала образуются β- или γ-сера превращающиеся позднее в α-серу с характерной зернистой структурой. При вулканических извержениях сера главным образом возникает при воздействии выделяющегося H 2
S на сернистый ангидрид или при окислении сероводорода кислородом воздуха; она может также возгоняться с парами воды. Пары S могут захватываться газами фумарол, струями углекислоты. Наблюдаемое впервые стадии вулканических извержений голубое пламя представляет облака горящей серы (Вулкано, на Липарских о-вах, Италия). Сероводородная стадия фумарол и сольфатар, сопровождающаяся образованием самородной серы, следует после стадии выделения фтористых и хлористых соединений и предшествует стадии углекислых выделений. Из сольфатар сера выделяется в виде рыхлых туфообразных продуктов, которые ветром и атмосферными осадками легко переносятся, образуя вторичные месторождения (Ков-Крик, шт. Юта в США).  Сера. Кристаллы в гипсе
Сера. Кристаллы в гипсе
Изменение минерала
В земной коре самородная сера легко окисляется с образованием серной кислоты и различных сульфатов; под влиянием бактерий может также давать сероводород.
Месторождения
Месторождения серы вулканического происхождения обычно невелики; они имеются на Камчатке (фумаролы), на горе Алагез в Армянии, в Италии (сольфатары Слит Поццуоли), в Исландии, Мексике, Японии, США, на Яве, на Липарских о-вах и т. д.
Выделение серы в горячих источниках сопровождается отложением опала, СаСО 3
, сульфатов и др. Местами сера замещает известняки около горячих источников, иногда выделяется в виде тончайшей мути. Горячие источники, отлагающие серу, наблюдаются в вулканических областях и в районах молодых тектонических нарушений, например, в России - на Кавказе, в Средней Азии, на Дальнем Востоке, на Курильских о-вах; в США - в Иеллоустонском национальном парке, в Калифорнии; в Италии, Испании, Японии и др.
Нередко самородная сера
образуется в процессе гипергенных изменений при разложении сульфидных минералов (пирита, марказита , мельниковита, галенита, антимонита и др.). Довольно большие скопления найдены в зоне окисления колчеданных залежей, например, в Сталинском месторождении Свердловской обл. и в Блявинском месторождении Оренбургской обл.; в последнем сера имеет вид плотной, но хрупкой массы слоистой текстуры, различной окраски. В месторождении Майкаин в Павлодарской области (Казахстан) крупные скопления самородной серы наблюдались между зоной ярозитов и зоной колчеданных руд.
В небольших количествах самородная сера встречается в зоне окисления очень многих месторождений. Известно образование серы в связи с каменноугольными пожарами при самовозгорании пирита или марказита (порошковатая сера в ряде месторождений Урала), при пожарах в месторождениях нефтеносных сланцев (например, в Калифорнии).
В черном морском иле сера образуется при его посерении на воздухе за счет изменения находящегося в нем односернистого железа.
Наиболее крупные промышленные месторождения серы находятся среди осадочных пород, главным образом третичного или пермского возраста. Их образование связано с восстановлением серы сульфатов, преимущественно гипса, реже - ангидрита. Вопрос о происхождении серы в осадочных образованиях является спорным. Гипс под влиянием органических соединений, бактерий, свободного водорода и др. восстанавливается сначала, возможно, до CaS или Ca(HS) 2
, которые под действием углекислоты и воды переходят в кальцит с выделением сероводорода; последний при взаимодействии с кислородом дает серу. Скопления серы в осадочных толщах иногда имеют пластовый характер. Часто они приурочены к соляным куполам. В этих месторождениях сера сопровождается асфальтом, нефтью, озокеритом, газообразными углеводородами, сероводородом, целестином, галитом, кальцитом, арагонитом, баритом, пиритом и другими минералами. Известны псевдоморфозы серы по волокнистому гипсу (селениту). В России такого типа месторождения имеются в районе Средней Волги (Сюкеевское Татарстан, Алекееевское, Водинское Самарская обл. и др.), в Туркменистане (Гаурдак, Каракумы), в Урало- Эмбенском р-не Казахстана, где ряд месторождений приурочен к соляным куполам, в Дагестане (Аварская и Махачкалинская группы) и в других районах.
Вне России крупные месторождения серы, приуроченные к осадочным толщам, имеются в Италии (Сицилия, Романья), в США (шт. Луизиана и Техас), Испании (около Кадиса) и в других странах.
Описание и свойства серы
Сера представляет собой вещество, которое находится в в 16 группе, под третьим периодом и имеет атомный номер – 16. Она может встретиться как в самородном, также и в связанном виде. Обозначается сера литерой S. Известна формула серы – (Ne)3s 2 3p 4 . Сера как элемент входит в состав многих белков.
На фото кристаллы серы
Если говорить о строении атома элемента серы , то на внешней его орбите есть электроны, валентное число которых достигает шести.
Это объясняет свойство элемента быть максимально шестивалентным в большинстве объединений. В структуре природного химического элемента есть четыре изотопа, и это – 32S, 33S, 34S и 36S. Говоря о внешней электронной оболочке, атом имеет схему 3s2 3р4. Радиус атома – 0,104 нанометра.
Свойства серы в первую очередь делятся на физического типа. К нему относится то, что элемент имеет твердый кристаллический состав. Два аллотропических видоизменения – основное состояние, в котором устойчив этот элемент серы.
Первое видоизменение ромбическое, имеющее лимонно-желтую окраску. Его устойчивость ниже, чем 95,6 °С. Второй – моноклинный, имеющий медово-желтую окраску. Его устойчивость колеблется от 95,6 °С и 119,3 °С.

На фото минерал сера
Во время плавки химический элемент стает движущейся жидкостью, имеющей желтый цвет. Она буреет, достигая температуры более 160 °С. А при 190 °С цвет серы превращается в темно-коричневый. После достижения отметки 190 °С наблюдается уменьшение вязкости вещества, которое все же после нагревания 300 °С стает жидкотекучим.
Другие свойства серы:
Практически не проводит тепла и электричества.
Не растворяется при погружении в воду.
Растворима в аммиаке, имеющем безводную структуру.
Также растворима в сероуглероде и других растворителях, имеющих органическую природу.
К характеристике элемента серы важно добавить и ее химические особенности. Она является активной в этом отношении. Если серу нагреть, то она может просто объединяться практически с любым химическим элементом.

На фото образец серы, добытый в Узбекистане
За исключением инертных газов. При контакте с металлами, хим. элемент образовывает сульфиды. Комнатная температура способствует тому, что элемент может вступить в реакцию с . Увеличенная температура способствует увеличению активности серы.
Рассмотрим, как поведение серы с отдельными веществами:
С металлами – является окислителем. Образовывает сульфиды.
С водородом – при высоких температурах – до 200 °С происходит активное взаимодействие.
С кислородом. Образовывается объединения оксидов при температурах до 280 °С.
С фосфором, углеродом – является окислителем. Только при отсутствии воздуха во время реакции.
С фтором – проявляет себя как восстановитель.
С веществами, имеющими сложную структуру – также как восстановитель.
Месторождения и добыча серы
Основной источник для получения серы – ее месторождения. В целом во всем мире насчитывается 1,4 млрд т запасов этого вещества. Ее добывают как при открытом и подземном способе выработки, так и с помощью выплавки из-под земли.

На фото добыча серы в вулкане Кава Иджен
Если применим последний случай, то используется вода, которую перегревают и расплавляют ею серу. В бедных рудах элемент содержится примерно в 12 %. Богатых – 25% и больше.
Распространенные типы месторождений:
Стратиформный – до 60%.
Солянокупольный – до 35 %.
Вулканогенный – до 5%.
Первый тип связан с толщами, несущими название сульфатно-карбонатных. При этом рудные тела, которые имеют мощность до нескольких десятков метров и с размером до сотни метров находятся в сульфатных породах.
Также эти пластовые залежи можно найти посреди пород сульфатного и карбонатного происхождения. Второй тип характеризуется залежами серого цвета, которые приурочиваются к соляным куполам.
Последний тип связывают с вулканами, имеющими молодую и современную структуру. При этом рудный элемент имеет пластообразную, линзовидную форму. В нем сера может содержаться в размере 40 %. Этот тип месторождения распространен в Тихоокеанском вулканическом поясе.
Месторождение серы в Евразии находится в Туркмении, в Поволжье и других местах. Породы серы находят возле левых берегов Волги, которые тянутся от Самары. Ширина полосы пород достигает нескольких километров. При этом их можно найти вплоть до Казани.

На фото сера в горной породе
В Техасе и Луизиане в кровлях соляных куполов находят огромное количество серы. Особо красивые Италийские этого элемента находят Романьи и Сицилии. А на острове Вулькано находят моноклинную серу. Элемент, который был окислен пиритом, нашли на Урале в Челябинской области.
Для добычи серы хим элемента используют разные способы. Все зависит от условия его залегания. При этом, конечно же, особое внимание уделяют безопасности.
Так как вместе с серной рудой скопляется сероводород, то необходимо особо серьезно подходить к любому способу добычи, ведь этот газ ядовитый для человека. Также и сера имеет свойство возгораться.
Чаще всего пользуются открытым способом. Так с помощью экскаваторов снимаются значительные части пород. Затем с помощью взрывов дробится рудная часть. Глыбы отправляются на фабрику для обогащения. Затем – на завод по плавке серы, где и получают серу из концентрата.

На фото сера в порту, привезенная морским транспортом
В случае глубокого залегания серы во многих объемах, используют метод Фраша. Сера расплавляется, находясь еще под землей. Затем, как и нефть выкачивается наружу через пробитую скважину. Такой подход основывается на том, что элемент легко плавится и имеет небольшую плотность.
Также известен способ разделения на центрифугах. Только этот способ имеет недостаток: сера получается с примесями. И тогда необходимо проводить ее дополнительную очистку.
В некоторых случаях используют скважный метод. Другие возможности добычи серного элемента:
Пароводяной.
Фильтрационный.
Термический.
Центрифугальный.
Экстракционный.
Применение серы
Большая часть добытой серы уходит, чтоб изготовить серную кислоту. А роль этого вещества очень огромная в химическом производстве. Примечательно, что для получения 1 тонны серного вещества необходимо 300 кг серы.
Бенгальские огни, которые ярко светятся и имеют много красителей, также производятся с помощью серы. Бумажная промышленность – это еще одна область, куда уходит значительная часть добытого вещества.

На фото серная мазь
Чаще всего применение сера находит при удовлетворении производственных нужд. Вот некоторые из них:
Использование в химическом производстве.
Для изготовления сульфитов, сульфатов.
Изготовление веществ для удобрения растений.
Чтоб получить цветные виды металлов.
Для придачи стали дополнительных свойств.
Для изготовления спичек, материалов для взрывов и пиротехники.
Краски, волокна из искусственных материалов – изготовляются при помощи этого элемента.
Для отбеливания ткани.
В некоторых случаях элемент сера входит в мази, которые лечат кожные болезни.
Цена серы
По последним новостям необходимость в сере активно растет. Стоимость на российский продукт равняется 130 долларам. На канадский вариант – 145 долларов. А вот в Ближнем Востоке цены возросли до 8 долларов, что привело к стоимости в 149 долларов.

На фото крупный экземпляр минерала сера
В аптеках можно найти молоту в порошок серу по цене от 10 до 30 рублей. К тому же есть возможность купить ее оптом. Некоторые организации предлагают по невысокой цене приобрести гранулированную техническую газовую серу .
В восточной части острова Ява, что находится в Индонезии, есть удивительное по красоте, но очень опасное по своей природе место – это вулкан Kawah Ijen. Вулкан находится на высоте около 2400 метров над уровнем море, диаметр его кратера 175 метров, а глубина – 212 метров. В его жерле расположено, наверное, самое странное и пугающее озеро прекрасного яблочно-изумрудного цвета, в котором рискнет искупаться разве что Терминатор, поскольку вместо воды в нем серная кислота. А точнее сказать – смесь серной и соляной кислоты объемом 40 млн. тонн.
Известный французский фотограф Оливье Грюневальда недавно совершил несколько путешествий в серные рудники в кратере вулкана Kawaha Ijen, находящегося в Восточной Яве, Индонезия. Там он сделал при помощи специального оборудования захватывающие сюрреалистичные фотографии этого места в лунном свете, освещенного факелами и синем пламенем горящей расплавленной серы.

Спуск в кальдеру вулкана Kawaha Ijen, где находится озеро с серной кислотой шириной в километр. На его берегах добывают серу
Каждый литр этой смертельной жижи содержит дополнительно по 5 грамм расплавленного алюминия. Всего же в озере по приблизительным подсчетам содержится более 200 тонн алюминия. На поверхности озерца температура колеблется в районе 60 градусов, а на его дне и все 200!

Кислые газы и пар выделяются из желтоватых кусков серы
Чтобы люди могли представить всю опасность озера для жизней своих, был проведен эксперимент. В озеро на 20 минут опустили лист алюминия, уже при погружении он стал покрываться пузырями, а по прошествии всего времени, алюминиевый лист стал тонким, словно кусок ткани.

Рабочий отламывает кусок от твердой серы. Потом серу несут на станцию взвешивания.
Однако озеро и сам кратер вулкана Kawah Ijen используется не для привлечения туристов, а для добычи серы в весьма неблагоприятных для человека условиях. А серы в этом кратере несметное количество, но поскольку это все же ЮВА, то полностью используется ручной труд.

Ночь. Шахтер с факелом находится внутри кратера вулкана Ijen Kawaha, глядя на поток жидкой серы, светящийся сверхъестественным голубым цветом.
Рабочие – местные жители без каких-либо защитных костюмов и противогазов, а вдыхать запах серы то еще отвращение, добывают куски серы день и ночь, используя при этом лишь свои ничем незащищенные руки и платок, повязанный на лице для защиты рта и носа.

Шахтеры трудятся здесь в адских условиях во время добычи серы. Фотограф Оливье Грюневальда описал здешний запах как невыносимый, требующий маску или противогаз для техники безопасности. Некоторые из горняков их носят, остальные работают без них.

Шахтеры с ломами, которыми откалывают куски серы:



Рабочий укладывает куски серы в корзины, чтобы выносить ее из вулкана:

Вам кажется это все нарисовано? Посмотрите видео:
Поверили?

Эти причудливые формы образовались из потока жидкой серы внутри кратера вулкана Kawaha Ijen. Когда сера расплавленная, она имеет кроваво-красный цвет. По мере охлаждения она становится все более и более желтой

Расплавленная сера капает из керамической трубы, которая конденсирует серные газы от вулкана в жидкость. Потом она остывает, затвердевает, и ее добывают рабочие







Шахтер дошел до пункта назначения со своим грузом. Шахтеры делают два или три ходки за серой в день, получая за свой тяжелый труд около $ 13 США за смену


Механизм для начальной переработки серы, где большие куски разбиваются на более мелкие

Затем куски серы помешаются над огнем, и она снова расплавляется

Расплавленная сера разливается по емкостям

Последний этап этогопроцесса - распределение жидкой серы на плитах для охлаждения. Когда она охладится и превратится в серные листы, они отправляются на местные местные заводы по вулканизации резины и других промышленные объекты









Фотограф Оливье Грюневальда: «Ощущение такое, что находишься на другой планете». Грюневальд потерял одну камеру и два объектива в суровых условиях кратера. Когда съемки были закончены, он выбросил все свои вещи в мусор: серный запах был настолько сильным, что от него невозможно будет избавиться.
А теперь дневной репортаж из этой шахты:

Индонезийский шахтер несет серу из Ijen 24 мая 2009 в окресностях Banyuwangi, Восточная Ява, Индонезия.

Заполненное кислотой озеро внутри кратера вулкана Ijen 200 метров в глубину и километр в ширину. Фото сделано 24 мая 2009 года в Восточной Яве, Индонезия. Озеро наполняется раствором серной кислоты и хлористого водорода при температуре 33 Сº.

Работник ремонтирует трубы, в которых, конденсируются сернистые газы. Комплекс вулкана Ijen 24 мая 2009 в окресностях Banyuwangi, Восточная Ява, Индонезия.

Шахтер извлекает серу из трубы на кратере вулкана Ijen 24 мая 2009 года в Восточной Яве, Индонезия. Расплавленная сера вытекает из труб глубокого красного цвета, и по мере охлаждения постепенно становится желтой и затвердевает.

Работники чинят трубы, в которых, конденсируются сернистые газы. Комплекс вулкана Ijen 24 мая 2009 в окресностях Banyuwangi, Восточная Ява, Индонезия.

Шахтер извлекает серу из трубы у кратера вулкана Ijen 24 мая 2009 года в Восточной Яве, Индонезия.

На этом фото, сделанном через сегмент запасной керамической трубы, работники ремонтируют большую трубу для конденсации серы. Комплекс вулкана Ijen 24 мая 2009 в окресностях Banyuwangi, Восточная Ява, Индонезия.


Кусок серы добываемой из вулкана Ijen. Фото сделано 24 мая 2009 год, Восточная Ява, Индонезия.

Шахтер извлекает серу из трубы на кратер вулкана Ijen 24 мая 2009 года в Восточной Яве, Индонезия.



Загруженные серой корзины, готовые к тому, чтобы их несли вверх по крутым стенам кратера, а затем до станции взвешивания. 24 мая 2009.


Шахтер приближается к верхней части стены кратера по исхоженной тропе, ведущей к вулкану Kawah Ijen 25 мая 2009 года в Восточной Яве, Индонезия.

На фото видно, как тяжела ноша – вес ее может доходить до 70кг - это заметно по сжатой коже и мышцам шахтера, который несет серу на станцию взвешивания 25 мая 2009.


Шахтер показывает болячки и шрамы от переноски серы из вулкана Ijen, 24 мая 2009 года в Восточной Яве, Индонезия.

Шахтер доходит до станции взвешивания и вешает свой груз серы на весы. 25 мая 2009 года в Восточной Яве, Индонезия.

Шахтер отдыхает на базовом лагере, который называется «Лагерь Sulfutara». 24 мая 2009 года в Индонезии.


Раздел 1. Определение серы.
Раздел 2. Природные минералы серы .
Раздел 3. История открытия серы .
Раздел 4. Происхождение названия сера.
Раздел 5. Происхождение серы.
Раздел 6. Получение серы.
Раздел 7. Производители серы.
Раздел 8. Свойства серы.
- Подраздел 1. Физические свойства.
- Подраздел 2. Химические свойства.
Раздел 10. Пожароопасные свойства серы.
- Подраздел 1. Пожары на складах серы.
Раздел 11. Нахождение в природе.
Раздел 12. Биологическая роль серы.
Раздел 13. Применение серы.
Определение серы
сера — это элемент шестой группы третьего периода периодической системы химических элементов Д. И. Менделеева, с атомным номером 16. Проявляет неметаллические свойства. Обозначается символом S (лат. Sulfur). В водородных и кислородных соединениях находится в составе различных ионов, образует многие кислоты и соли. Многие серосодержащие соли малорастворимы в воде.
Сера - S, химический элемент с атомным номером 16, атомная масса 32,066. Химический символ серы S произносится «эс». Природная сера состоит из четырех стабильных нуклидов: 32S (содержание 95,084% по массе), 33S (0,74 %), 34S (4,16%) и 36S (0,016 %). Радиус атома серы 0,104 нм. Радиусы ионов: иона S2- 0,170 нм (координационное число 6), иона S4+ 0,051 нм (координационное число 6) и иона S6+ 0,026 нм (координационное число 4). Энергии последовательной ионизации нейтрального атома серы от S0 до S6+ равны, соответственно, 10,36, 23,35, 34,8, 47,3, 72,5 и 88,0 эВ. Сера расположена в VIA группе периодической системы Д. И. Менделеева, в 3-м периоде, и принадлежит к числу халькогенов. Конфигурация внешнего электронного слоя 3s23p4. Наиболее характерны степени окисления в соединениях -2, +4, +6 (валентности соответственно II, IV и VI). Значение электроотрицательности серы по Полингу 2,6. Сера относится к числу неметаллов.


В свободном виде сера представляет собой желтые хрупкие кристаллы или желтый порошок.
Сера (Sulfur) - это
Природные минералы серы
Сера является шестнадцатым по химической распространённости элементом в земной коре. Встречается в свободном (самородном) состоянии и связанном виде.
Важнейшие природные соединения серы: FeS2 — железный колчедан или пирит, ZnS — цинковая обманка или сфалерит (вюрцит), PbS — свинцовый блеск или галенит, HgS — киноварь, Sb2S3 — антимонит. Кроме того, сера присутствует в черного золота, природном угле, природных газах и сланцах. Сера — шестой элемент по содержанию в природных водах, встречается в основном в виде сульфат-иона и обуславливает «постоянную» жёсткость пресной воды. Жизненно важный элемент для высших организмов, составная часть многих белков, концентрируется в волосах.








Сера (Sulfur) - это
История открытия серы
сера в самородном состоянии, а также в виде сернистых соединений известна с древнейших времён. С запахом горящей серы, удушающим действием сернистого газа и отвратительным запахом сероводорода человек познакомился, вероятно, ещё в доисторические времена. Именно из-за этих свойств сера использовалась жрецами в составе священных курений при религиозных обрядах. Сера считалась произведением сверхчеловеческих существ из мира духов или подземных богов. Очень давно сера стала применяться в составе различных горючих смесей для военных целей. Уже у Гомера описаны «сернистые испарения», смертельное действие выделений горящей серы. Сера, вероятно, входила в состав «греческого огня», наводившего ужас на противников. Около VIII в. китайцы стали использовать её в пиротехнических смесях, в частности, в смеси типа пороха. Горючесть серы, лёгкость, с которой она соединяется с металлами с образованием сульфидов (например, на поверхности кусков металла ), объясняют то, что её считали «принципом горючести» и обязательной составной частью металлических руд. Пресвитер Теофил (XII в.) описывает способ окислительного обжига сульфидной медной руды, известный, вероятно, ещё в древнем Египте. В период арабской алхимии возникла ртутно-серная теория состава металлов , согласно которой сера почиталась обязательной составной частью (отцом) всех металлов. В дальнейшем она стала одним из трёх принципов алхимиков, а позднее «принцип горючести» явился основой теории флогистона. Элементарную природу серы установил Лавуазье в своих опытах по сжиганию. С введением пороха в Европе началось развитие добычи природной серы, а также разработка способа получения её из пиритов; последний был распространён в древней Руси. Впервые в литературе он описан у Агриколы. Таким образом, точно происхождение серы не установлено, но, как сказано выше, этот элемент использовался до Рождества Христова, а значит знаком людям с давних времён.


Сера встречается в природе в свободном (самородном) состоянии, поэтому она была известна человеку уже в глубокой древности. Сера привлекала внимание характерной окраской, голубым цветом пламени и специфическим запахом, возникающим при горении (запах сернистого газа). Считалось, что горящая сера отгоняет нечистую силу. В Библии говорится об использовании серы для очищения грешников. У человека средневековья запах «серы» ассоциировался с преисподней. Применение горящей серы для дезинфекции упоминается Гомером. В Древнем Риме с помощью сернистого газа отбеливали ткани.
Издавна использовалась сера в медицине — ее пламенем окуривали больных, ее включали в состав различных мазей для лечения кожных заболеваний. В 11 в. Авиценна (Ибн Сина), а затем и европейские алхимики полагали, что металлы, в том числе и серебро, состоят из находящихся в различных соотношениях серы и ртути. Поэтому сера играла важную роль в попытках алхимиков найти «философский камень» и превратить недрагоценные металлы в драгоценные. В 16 в. Парацельс считал серу наряду с ртутью и «солью» одним из основных «начал» природы, «душою» всех тел.

Практическое значение серы резко возросло после того, как изобрели черный порох (в состав которого обязательно входит сера). Византийцы в 673 г., защищая Константинополь, сожгли флот неприятеля с помощью так называемого греческого огня - смеси селитры, серы, смолы и других веществ — пламя которого не гасилось водой. В средние века в Европе применялся черный порох, по составу близкий к смеси греческого огня. С тех пор началось широкое использование серы для военных целей.

Издавна было известно и важнейшее соединение серы — серная кислота. Один из создателей ятрохимии, монах Василий Валентин, в 15 веке подробно описал получение серной кислоты путем прокаливания железного купороса (старинное название серной кислоты — купоросное масло).

Элементарную природу серы установил в 1789 А. Лавуазье. В названиях химических соединений, содержащих серу, часто содержится приставка «тио» (например, применяемый в фотографии реактив Na2S2O3 имеет название тиосульфат натрия). Происхождение этой приставки связано с греческим названием серы — theion.
Происхождение названия сера
Русское название серы восходит к праславянскому *sěra, которое связывают с лат. sērum «сыворотка».
Латинское sulphur (эллинизированное написание более старого sulpur) восходит к индоевропейскому корню *swelp- «гореть».
Происхождение серы
Большие скопления самородной серы встречаются не так уж часто. Чаще она присутствует в некоторых рудах. Руда самородной серы — это порода с вкраплениями чистой серы.
Когда образовались эти вкрапления — одновременно с сопутствующими породами или позже? От ответа на этот вопрос зависит направление поисковых и разведочных работ. Но, несмотря на тысячелетия общения с серой, человечество до сих пор не имеет однозначного ответа. Существует несколько теорий, авторы которых придерживаются противоположных взглядов.
Теория сингенеза (то есть одновременного образования серы и вмещающих пород) предполагает, что образование самородной серы происходило в мелководных бассейнах. Особые бактерии восстанавливали сульфаты, растворённые в воде, до сероводорода, который поднимался вверх, попадал в окислительную зону и здесь химическим путём или при участии других бактерий окислялся до элементарной серы. Сера осаждалась на дно, и впоследствии содержащий серу ил образовал руду.
Теория эпигенеза (вкрапления серы образовались позднее, чем основные породы) имеет несколько вариантов. Самый распространённый из них предполагает, что подземные воды, проникая сквозь толщи пород, обогащаются сульфатами. Если такие воды соприкасаются с месторождениями черного золота или Природного газа, то ионы сульфатов восстанавливаются углеводородами до сероводорода. Сероводород поднимается к поверхности и, окисляясь, выделяет чистую серу в пустотах и трещинах пород.
В последние десятилетия находит всё новые подтверждения одна из разновидностей теории эпигенеза — теория метасоматоза (в переводе с греческого «метасоматоз» означает замещение). Согласно ей в недрах постоянно происходит превращение гипса CaSO4-H2O и ангидрита CaSO4 в серу и кальцит СаСО3. Эта теория создана в 1935 году советскими учёными Л. М. Миропольским и Б. П. Кротовым. В её пользу говорит, в частности, такой факт.

В 1961 году в Ираке было открыто Мишрак. Сера здесь заключена в карбонатных породах, которые образуют свод, поддерживаемый уходящими вглубь опорами (в геологии их называют крыльями). Крылья эти состоят в основном из ангидрита и гипса. Такая же картина наблюдалась на отечественном месторождении Шор-Су.
Геологическое своеобразие этих месторождений можно объяснить только с позиций теории метасоматоза: первичные гипсы и ангидриты превратились во вторичные карбонатные руды с вкраплениями самородной серы. Важно не только соседство минералов — среднее содержание серы в руде этих месторождений равно содержанию химически связанной серы в ангидрите. А исследования изотопного состава серы и углерода в руде этих месторождений дали сторонникам теории метасоматоза дополнительные аргументы.

Но есть одно «но»: химизм процесса превращения гипса в серу и кальцит пока не ясен, и потому нет оснований считать теорию метасоматоза единственно правильной. На земле и сейчас существуют озёра (в частности, Серное озеро близ Серноводска), где происходит сингенетическое отложение серы и сероносный ил не содержит ни гипса, ни ангидрита.

Всё это означает, что разнообразие теорий и гипотез о происхождении самородной серы — результат не только и не столько неполноты наших знаний, сколько сложности явлений, происходящих в недрах . Ещё из элементарной школьной математики все мы знаем, что к одному результату могут привести разные пути. Этот распространяется и на геохимию.
Получение серы
серу получают главным образом выплавкой самородной серы непосредственно в местах её залегания под землёй. Серные руды добывают разными способами — в зависимости от условий залегания. Залежам серы почти всегда сопутствуют скопления ядовитых газов — соединений серы. К тому же нельзя забывать о возможности её самовозгорания.
Добыча руды открытым способом происходит так. Шагающие экскаваторы снимают пласты пород, под которыми залегает руда. Взрывами рудный пласт дробят, после чего глыбы руды отправляют на сероплавильный завод, где из концентрата извлекают серу.
В 1890 г. Герман Фраш, предложил плавить серу под землёй и через скважины, подобные нефтяным, выкачивать её на поверхность. Сравнительно невысокая (113°C) температура плавления серы подтверждала реальность идеи Фраша. В 1890 г. начались испытания, приведшие к успеху.
Известно несколько методов получения серы из серных руд: пароводяные, фильтрационные, термические, центрифугальные и экстракционные.
Также сера в больших количествах содержится в Природном газе в газообразном состоянии (в виде сероводорода, сернистого ангидрида). При добыче она откладывается на стенках труб и оборудования, выводя их из строя. Поэтому её улавливают из газа как можно быстрее после добычи. Полученная химически чистая мелкодисперсная сера является идеальным сырьём для химической и резиновой промышленности.
Крупнейшее месторождение самородной серы вулканического происхождения находится на острове Итуруп с запасами категории A+B+C1 - 4227 тыс. тонн и категории C2 - 895 тыс. тонн, что достаточно для строительства предприятия мощностью 200 тыс. тонн гранулированной серы в год.

Производители серы
Основными производителями серы в Российской Федерации являются предприятия ОАО Газпром: ООО Газпром добыча Астрахань и ООО Газпром добыча Оренбург, получающие её как побочный при очистке газа.

Свойства серы
1) Физические
сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов. Наиболее стабильны циклические молекулы S8, имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера — хрупкое вещество жёлтого цвета. Кроме того, возможны молекулы с замкнутыми (S4, S6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета, которая получается при резком охлаждении расплава серы (пластическая сера уже через несколько часов становится хрупкой, приобретает жёлтый цвет и постепенно превращается в ромбическую). Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами. В воде сера нерастворима, некоторые её модификации растворяются в органических растворителях, например сероуглероде, скипидаре. Плавление серы сопровождается заметным увеличением объёма (примерно 15 %). Расплавленная сера представляет собой жёлтую легкоподвижную жидкость, которая выше 160 °C превращается в очень вязкую тёмно-коричневую массу. Наибольшую вязкость расплав серы приобретает при температуре 190 °С; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °С полимерные звенья начинают рушиться. Сера может служить простейшим примером электрета. При трении сера приобретает сильный отрицательный заряд.


Серу применяют для производства серной кислоты, вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная — лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента — для получения серобетона.



2) Химические
Горение серы
На воздухе сера горит, образуя сернистый ангидрид — бесцветный газ с резким запахом:
С помощью спектрального анализа установлено, что на самом деле процесс окисления серы в двуокись представляет собой цепную реакцию и происходит с образованием ряда промежуточных продуктов: моноокиси серы S2O2, молекулярной серы S2, свободных атомов серы S и свободных радикалов моноокиси серы SO.

Помимо кислорода, сера реагирует со многими неметаллами, однако при комнатной температуре сера - только со фтором, проявляя восстановительные свойства:
Расплав серы реагирует с хлором, при этом возможно образование двух низших хлоридов:
2S + Cl2 = S2Cl2
При нагревании сера также реагирует с фосфором, образуя, видимо, смесь сульфидов фосфора, среди которых — высший сульфид P2S5:
Кроме того, при нагревании сера реагирует с водородом, углеродом, кремнием:
S + H2 = H2S (сероводород)
C + 2S = CS2 (сероуглерод)


При нагревании сера взаимодействует со многими металлами, часто — весьма бурно. Иногда смесь металла с серой загорается при поджигании. При этом взаимодействии образуются сульфиды:
2Al + 3S = Al2S3
Растворы сульфидов щелочных металлов реагируют с серой с образованием полисульфидов:
Na2S + S = Na2S2
Из сложных веществ следует отметить прежде всего реакцию серы с расплавленной щёлочью, в которой сера диспропорционирует аналогично хлору:
3S + 6KOH = K2SO3 + 2K2S + 3H2O
Полученный плав называется серной печенью.

С концентрированными кислотами-окислителями (HNO3, H2SO4) сера реагирует только при длительном нагревании, окисляясь:
S + 6HNO3(конц.) = H2SO4 + 6NO2 + 2H2O
S + 2H2SO4(конц.) = 3SO2 + 2H2O
Сера (Sulfur) - это
Сера (Sulfur) - это
Пожароопасные свойства серы
Тонкоизмельченная сера склонна к химическому самовозгоранию в присутствии влаги, при контакте с окислителями, а также в смеси с углём, жирами, маслами. Сера образует взрывчатые смеси с нитратами, хлоратами и перхлоратами. Самовозгорается при контакте с хлорной известью.
Средства тушения: распылённая вода, воздушно-механическая пена.


По данным В. Маршалла пыль серы относится к разряду взрывоопасных, но для взрыва необходима достаточно высокая концентрация пыли — порядка 20 г/м3 (20000мг/м3), такая концентрация во много раз превышает предельно допустимую концентрацию для человека в воздухе рабочей зоны — 6 мг/м3.
Пары образуют с воздухом взрывчатую смесь.
Горение серы протекает только в расплавленном состоянии аналогично горению жидкостей. Верхний слой горящей серы кипит, создавая пары, которые образуют слабосветящееся пламя высотой до 5 см. Температура пламени при горении серы составляет 1820 °C.
Так как воздух по объёму состоит приблизительно из 21 % кислорода и 79 % азота и при горении серы из одного объёма кислорода получается один объём SO2, то максимальное теоретически возможное содержание SO2 в газовой смеси составляет 21 %. На практике горение происходит с некоторым избытком воздуха, и объёмное содержание SO2 в газовой смеси меньше теоретически возможного, составляя обычно 14…15 %.
Обнаружение горения серы пожарной автоматикой является трудной проблемой. Пламя сложно обнаружить человеческим глазом или видеокамерой, спектр голубого пламени лежит в основном в ультрафиолетовом диапазоне. Горение происходит при низкой температуре. Для обнаружения горения тепловым извещателем необходимо размещать его непосредственно близко к сере. Пламя серы не излучает в инфракрасном диапазоне. Таким образом оно не будет обнаружено распространёнными инфракрасными извещателями. Ими будут обнаруживаться лишь вторичные возгорания. Пламя серы не выделяет паров воды. Таким образом детекторы ультрафиолетовых извещателей пламени, использующие соединения никеля, не будут работать.
Для выполнения требований пожарной безопасности на складах серы необходимо:
Конструкции и технологическое оборудование должны регулярно очищаться от пыли;
Помещение склада должно постоянно проветриваться естественной вентиляцией при открытых дверях;
Дробление комков серы на решётке бункера должно производиться деревянными кувалдами или инструментом из неискрящего материала;
Конвейеры для подачи серы в производственные помещения должны быть снабжены металлоискателями;
В местах хранения и применения серы необходимо предусматривать устройства (бортики, пороги с пандусом и т. п.), обеспечивающие в аварийной ситуации предотвращение растекания расплава серы за пределы помещения или открытой площадки;
На складе серы запрещается:
Производство всех видов работ с применением открытого огня;
Складировать и хранить промасленную ветошь и тряпки;
При ремонте применять инструмент из искродающего материала.
Пожары на складах серы
В декабре 1995 года на открытом складе серы предприятия , расположенного в городе Сомерсет Вест Западной Капской провинции Южно-Африканской Республики произошёл крупный пожар, погибли два человека.
16 января 2006 г. около пяти вечера на череповецком предприятии «Аммофос» загорелся склад с серой. Общая площадь пожара — около 250-ти квадратных метров. Полностью ликвидировать его удалось лишь в начале второго ночи. Жертв и пострадавших нет.
15 марта 2007 рано утром на ООО «Балаковский завод волоконных материалов» произошёл пожар на закрытом складе серы. Площадь пожара составила 20 кв.м. На пожаре работало 4 пожарных расчёта с личным составом в 13 человек. Примерно через полчаса пожар был ликвидирован. Никто не пострадал.
4 и 9 марта 2008 года произошло возгорание серы в Атырауской области в хранилище серы ТШО на Тенгизском месторождении. В первом случае очаг возгорания удалось потушить быстро, во втором случае сера горела 4 часа. Объём горевших отходов нефтепереработки, к каковым по казахстанским законам отнесена сера, составил более 9 тысяч килограммов.
В апреле 2008 недалеко от посёлка Кряж Самарской области загорелся склад, на котором хранилось 70 тонн серы. Пожару была присвоена вторая категория сложности. К месту происшествия выехали 11 пожарных расчётов и спасатели. В тот момент, когда пожарные оказались около склада, горела ещё не вся сера, а только её небольшая часть — около 300 килограммов. Площадь возгорания вместе с участками сухой травы, прилегающими к складу, составила 80 квадратных метров. Пожарным удалось быстро сбить пламя и локализовать пожар: очаги возгорания были засыпаны землёй и залиты водой.
В июле 2009 в Днепродзержинске горела сера. Пожар произошёл на одном из коксохимических предприятий в Баглейском районе города. Огонь охватил более восьми тонн серы. Никто из сотрудников комбината не пострадал.
Нахождение в природе серы
С ера довольно широко распространена в природе. В земной коре ее содержание оценивается в 0,05% по массе. В природе часто встречаются значительные залежи самородной серы (обычно вблизи вулканов); в Европе они расположены на юге Италии, в Сицилии. Еще большие залежи самородной серы имеются в США (в штатах Луизиана и Техас), а также в Средней Азии, в Японии, в Мексике. В природе сера встречается как россыпями, так и в виде кристаллических пластов, иногда образуя изумительные по красоте группы полупрозрачных желтых кристаллов (так называемые друзы).


В вулканических местностях часто наблюдается выделение из-под земли газа сероводорода H2S; в этих же регионах сероводород встречается в растворенном виде в серных водах. Вулканические газы часто содержат также сернистый газ SO2.
На поверхности нашей планеты широко распространены месторождения различных сульфидных соединений. Наиболее часто среди них встречаются: железный колчедан (пирит) FeS2, медный колчедан (халькопирит) CuFeS2, свинцовый блеск PbS, киноварь HgS, сфалерит ZnS и его кристалическая модификация вюртцит, антимонит Sb2S3 и другие. Известны также многочисленные месторождения различных сульфатов, например, сульфата кальция (гипс CaSO4·2H2O и ангидрит CaSO4), сульфата магния MgSO4 (горькая соль), сульфата бария BaSO4 (барит), сульфата стронция SrSO4 (целестин), сульфата натрия Na2SO4·10H2O (мирабилит) и др.




Каменные угли содержат в среднем 1,0-1,5% серы. Сера может входить и в состав черного золота . Целый ряд месторождений природного горючего газа (например, Астраханское) содержат как примесь сероводород.

Сера относится к элементам, которые необходимы для живых организмов, так как она является существенной составной частью белков. Белки содержат 0,8-2,4% (по массе) химически связанной серы. Растения получают серу из сульфатов, содержащихся в почве. Неприятные запахи, возникающие при гниении трупов животных, объясняются главным образом выделением соединений серы (сероводорода: и меркаптанов), образующихся при разложении белков. В морской воде присутствует около 8,7·10-2 % серы.
Получение серы
С еру получают, в основном, выплавляя ее из горных пород, содержащих самородную (элементарную) серу. Так называемый геотехнологический способ позволяет получать серу без подъема руды на поверхность. Этот способ был предложен в конце 19 века американским химиком Г. Фрашем, перед которым встала задача извлечения на поверхность земли серы из месторождений юга США , где песчаный грунт резко усложнял ее добычу традиционным шахтным методом.
Фраш предложил использовать для подъема серы на поверхность перегретый водяной пар. Перегретый пар по трубе подают в подземный слой, содержащий серу. Сера плавится (ее температура плавления немного ниже 120°С) и по трубе, расположенной внутри той, по которой под землю закачивают водяной пар, поднимается наверх. Для того чтобы обеспечить подъем жидкой серы, через самую тонкую внутреннюю трубу нагнетают сжатый воздух.
По другому (термическому) методу, получившему особое распространение в начале 20 века на Сицилии, серу выплавляют, или возгоняют, из дробленной горной породы в специальных глиняных печах.
Существуют и другие методы выделения самородной серы из породы, например, экстракцией сероуглеродом или флотационными методами.
В связи с тем, что потребность промышленности в сере очень велика, разработаны методы ее получения из сероводорода H2S и сульфатов.
Метод окисления сероводорода до элементарной серы был впервые разработан в Великобритании, где значительные количества серы научились получать из остающегося после получении соды Na2CO3 по методу французского химика Н. Леблана сульфида кальция CaS. Метод Леблана основан на восстановлении сульфата натрия углем в присутствии известняка CaCO3.
Na2SO4 + 2C = Na2S + 2CO2;
Na2S + CaCO3 = Na2CO3 + CaS.
Соду затем выщелачивают водой, а водную суспензию плохо растворимого сульфида кальция обрабатывают диоксидом углерода:
CaS + CO2 + H2O = CaCO3 + H2S
Образующийся сероводород H2S в смеси с воздухом пропускают в печи над слоем катализатора. При этом за счет неполного окисления сероводорода образуется сера:
2H2S + O2 = 2H2O +2S
Аналогичный метод используют для получения элементарной серы и из сероводорода, сопутствующего природным газам.
Так как современная техника нуждается в сере высокой чистоты, разработаны эффективные методы рафинирования серы. При этом используют, в частности, различия в химическом поведении серы и примесей. Так, мышьяк и селен удаляют, обработав серу смесью азотной и серной кислот.
Использованием методов, основанных на дистилляции и ректификации, удается получить высокочистую серу с содержанием примесей 10-5 - 10-6 % по массе.
Применение серы
О коло половины производимой серы используется на производство серной кислоты, около 25% расходуется для получения сульфитов, 10-15% — для борьбы с вредителями сельскохозяйственных культур (главным образом винограда и хлопчатника) (наибольшее значение здесь имеет раствор медного купороса CuSO4·5H2O), около 10% используется резиновой промышленностью для вулканизации резины. Серу применяют при производстве красителей и пигментов, взрывчатых веществ (она до сих пор входит в состав пороха), искусственных волокон, люминофоров. Серу используют при производстве спичек, так как она входит в состав, из которого изготовляют головки спичек. Серу до сих пор содержат некоторые мази, которыми лечат заболевания кожи. Для придания сталям особых свойств в них вводят небольшие добавки серы (хотя, как правило, примесь серы в сталях нежелательна).




Биологическая роль серы
С ера постоянно присутствует во всех живых организмах, являясь важным биогенным элементом. Ее содержание в растениях составляет 0,3-1,2 %, в животных 0,5-2 % (морские организмы содержат больше серы, чем наземные). Биологическое значение серы определяется прежде всего тем, что она входит в состав аминокислот метионина и цистеина и, следовательно, в состав пептидов и белков. Дисульфидные связи -S-S- в полипетидных цепях участвуют в формировании пространственной структуры белков, а сульфгидрильные группы (-SH) играют важную роль в активных центрах ферментов. Кроме того, сера входит в молекулы гормонов, важных веществ. Много серы содержится в кератине волос, костях, нервной ткани. Неорганические соединения серы необходимы для минерального питания растений. Они служат субстратами окислительных реакций, осуществляемых распространенными в природе серобактериями.
В организме среднего человека (масса тела 70 кг) содержится около 1402 г серы. Суточная потребность взрослого человека в сере — около 4.
Однако по своему отрицательному воздействию на окружающую среду и человека сера (точнее, ее соединения) стоит на одном из первых мест. Основной источник загрязнения серой — сжигание каменного угля и других видов топлива, содержащих серу. При этом около 96% серы, содержащейся в топливе, попадает в атмосферу в виде сернистого газа SO2.
В атмосфере сернистый газ постепенно окисляется до оксида серы (VI). Оба оксида — и оксид серы (IV), и оксид серы (VI) — взаимодействуют с парами воды с образованием кислотного раствора. Затем эти растворы выпадают в виде кислотных дождей. Оказавшись в почве, кислотные воды угнетают развитие почвенной фауны и растений. В результате создаются неблагоприятные условия для развития растительности, особенно в северных регионах, где к суровому климату добавляется химическое загрязнение. В результате гибнут леса, нарушается травяной покров, ухудшается состояние водоемов. Кислотные дожди разрушают изготовленные из мрамора и других материалов памятники, более того, они вызывают разрушение даже каменных зданий и предметов торговли из металлов. Поэтому приходится принимать разнообразные меры по предотвращению попадания соединений серы из топлива в атмосферу. Для этого подвергают очистке от соединений серы и нефтепродукты, очищают образующиеся при сжигании топлива газы.

Сама по себе сера в виде пыли раздражает слизистые оболочки, органы дыхания и может вызывать серьезные заболевания. ПДК серы в воздухе 0,07 мг/м3.
Многие соединения серы токсичны. Особенно следует отметить сероводород, вдыхание которого быстро вызывает притупление реакции на его неприятный запах и может привести к тяжелым отравлениям даже с летальным исходом. ПДК сероводорода в воздухе рабочих помещений 10 мг/м3, в атмосферном воздухе 0,008 мг/м3.
Источники
Химическая энциклопедия: в 5 т. / Редкол.:Зефиров Н. С. (гл. ред.). — Москва: Советская энциклопедия, 1995. — Т. 4. — С. 319. — 639 с. — 20 000 экз. — ISBN 5—85270—039—8
Большая медицинская энциклопедия
СЕРА - хим. элемент, символ S (лат. Sulfur), ат. н. 16, ат. м. 32,06. Существует в виде нескольких аллотропных модификаций; среди них сера моноклинной модификации (плотность 1960 кг/м3, tпл = 119°С) и ромбическая сера (плотность 2070 кг/м3, ίπι = 112,8… … Большая политехническая энциклопедия
СЕРА - (обозначается S), химический элемент VI группы ПЕРИОДИЧЕСКОЙ ТАБЛИЦЫ, неметалл, известный с древности. Встречается в природе как в виде отдельного элемента, так и в виде сульфидных минералов, таких как ГАЛЕНИТ и ПИРИТ, и сульфатных минералов,… … Научно-технический энциклопедический словарь
сера - В мифологии ирландских кельтов Сера отец Парталона (см. глава 6). Согласно некоторым источникам, именно Сера, а не Парталон был мужем Дилгнейд. (
Чистая желтая сера
Минерал из класса самородных элементов. Сера представляет собой пример хорошо выраженного энантиоморфного полиморфизма. В природе образует 2 полиморфные модификации: a-сера ромбическая и b-сера моноклинная. При атмосферном давлении и температуре 95,6°С a-сера переходит в b-серу. Сера жизненно необходима для роста растений и животных, она входит в состав живых организмов и продуктов их разложения, ее много, например, в яйцах, капусте, хрене, чесноке, горчице, луке, волосах, шерсти и т.д. Она присутствует также в углях и нефти.
Смотрите так же:
СТРУКТУРА

Самородная сера обычно представлена a-серой, которая кристаллизуется в ромбической сингонии, ромбо-дипирамидальный вид симметрии. Кристаллическая сера имеет две модификации; одну из них, ромбическую, получают из раствора серы в сероуглероде (CS 2) испарением растворителя при комнатной температуре. При этом образуются ромбовидные просвечивающие кристаллы светложелтого цвета, легко растворимые в CS 2 . Эта модификация устойчива до 96° С, при более высокой температуре стабильна моноклинная форма. При естественном охлаждении расплавленной серы в цилиндрических тиглях вырастают крупные кристаллы ромбической модификации с искаженной формой (октаэдры, у которых частично «срезаны» углы или грани). Такой материал в промышленности называется комовая сера. Моноклинная модификация серы представляет собой длинные прозрачные темножелтые игольчатые кристаллы, также растворимые в CS 2 . При охлаждении моноклинной серы ниже 96° С образуется более стабильная желтая ромбическая сера.
СВОЙСТВА

Самородная сера жёлтого цвета, при наличии примесей — жёлто-коричневая, оранжевая, бурая до чёрной; содержит включения битумов, карбонатов, сульфатов, глины. Кристаллы чистой серы прозрачны или полупрозрачны, сплошные массы просвечивают в краях. Блеск смолистый до жирного. Твердость 1-2, спайности нет, излом раковистый. Плотность 2,05 -2,08 г/см 3 , хрупкая. Легко растворима в канадском бальзаме, в скипидаре и керосине. В HCl и H 2 SO 4 нерастворима. HNO 3 и царская водка окисляют серу, превращая её в H 2 SO 4 . Сера существенно отличается от кислорода способностью образовывать устойчивые цепочки и циклы из атомов.
Наиболее стабильны циклические молекулы S 8 , имеющие форму короны, образующие ромбическую и моноклинную серу. Это кристаллическая сера - хрупкое вещество жёлтого цвета. Кроме того, возможны молекулы с замкнутыми (S 4 , S 6) цепями и открытыми цепями. Такой состав имеет пластическая сера, вещество коричневого цвета, которая получается при резком охлаждении расплава серы (пластическая сера уже через несколько часов становится хрупкой, приобретает жёлтый цвет и постепенно превращается в ромбическую). Формулу серы чаще всего записывают просто S, так как она, хотя и имеет молекулярную структуру, является смесью простых веществ с разными молекулами.
Плавление серы сопровождается заметным увеличением объёма (примерно 15 %). Расплавленная сера представляет собой жёлтую легкоподвижную жидкость, которая выше 160 °C превращается в очень вязкую тёмно-коричневую массу. Наибольшую вязкость расплав серы приобретает при температуре 190 °C; дальнейшее повышение температуры сопровождается уменьшением вязкости и выше 300 °C расплавленная сера снова становится подвижной. Это связано с тем, что при нагревании серы она постепенно полимеризуется, увеличивая длину цепочки с повышением температуры. При нагревании серы свыше 190 °C полимерные звенья начинают рушиться.
Сера может служить простейшим примером электрета. При трении сера приобретает сильный отрицательный заряд.
МОРФОЛОГИЯ

Образует усечённо-дипирамидальные, реже дипирамидальные, пинакоидальные или толстопризматические кристаллы, а также плотные скрытокристаллические, сливные, зернистые, реже тонковолокнистые агрегаты. Главные формы на кристаллах: дипирамиды (111) и (113), призмы (011) и (101), пинакоид (001). Также сростки и друзы кристаллов, скелетные кристаллы, псевдосталактиты, порошковатые и землистые массы, налёты и примазки. Для кристаллов характерны множественные параллельные срастания.
ПРОИСХОЖДЕНИЕ

Сера образуется при вулканических извержениях, при выветривании сульфидов, при разложении гипсоносных осадочных толщ, а также в связи с деятельностью бактерий. Главные типы месторождений самородной серы — вулканогенные и экзогенные (хемогенно-осадочные). Экзогенные месторождения преобладают; они связаны с гипсо-ангидритами, которые под воздействием выделений углеводородов и сероводорода восстанавливаются и замещаются серно-кальцитовыми рудами. Такой инфильтрационно-метасоматический генезис имеют все крупнейшие месторождения. Самородная сера часто образуется (кроме крупных cкоплений) в результате окисления H 2 S. Геохимические процессы её образования существенно активизируются микроорганизмами (сульфатредуцирующими и тионовыми бактериями). Сопутствующие минералы — кальцит, арагонит, гипс, ангидрит, целестин, иногда битумы. Среди вулканогенных месторождений самородной серы главное значение имеют гидротермально-метасоматические (например, в Японии), образованные сероносными кварцитами и опалитами, и вулканогенно-осадочные сероносные илы кратерных озёр. Образуется также при фумарольной деятельности. Образуясь в условиях земной поверхности, самородная сера является всё же не очень устойчивой и, постепенно окисляясь, даёт начало сульфатам, гл. образом гипсу.
Используется в производстве серной кислоты (около 50% добываемого количества). В 1890 г. Герман Фраш предложил плавить серу под землёй и извлекать на поверхность через скважины, и в настоящее время месторождения серы разрабатывают главным образом путём выплавки самородной серы из пластов под землёй непосредственно в местах её залегания. Сера также в больших количествах содержится в природном газе (в виде сероводорода и сернистого ангидрида), при добыче газа она откладывается на стенках труб, выводя их из строя, поэтому её улавливают из газа как можно быстрее после добычи.
ПРИМЕНЕНИЕ

Примерно половина производимой серы используется в производстве серной кислоты. Серу применяют для вулканизации каучука, как фунгицид в сельском хозяйстве и как сера коллоидная - лекарственный препарат. Также сера в составе серобитумных композиций применяется для получения сероасфальта, а в качестве заместителя портландцемента - для получения серобетона. Сера находит применение для производства пиротехнических составов, ранее использовалась в производстве пороха, применяется для производства спичек.
Сера (англ. Sulphur) — S
КЛАССИФИКАЦИЯ
| Strunz (8-ое издание) | 1/B.03-10 |
| Nickel-Strunz (10-ое издание) | 1.CC.05 |
| Dana (7-ое издание) | 1.3.4.1 |
| Dana (8-ое издание) | 1.3.5.1 |
| Hey’s CIM Ref. | 1.51 |